科学的な解析(化学)を行う際には基本的に反応物質の分子量や酸化数や電離式などの理解が必要となることが多いです。
そのためさまざまな物質の分子量や酸化数や電離式を理解しておくといいわけですが、あなた覚えられていますか。
ここでは代表的な化学物質のCO2(二酸化炭素)に着目して、その分子式、構造式、電子式、分子構造、極性などをまとめていきますので、参考にしてみてください。
CO2の分子式は?【二酸化炭素の分子式】
二酸化炭素の分子は炭素原子(C)1つと酸素原子(O)2つが結合しCO2と表される化合物です。

基本的にCO2を始めとして、化学式ではその後ろの文字や数値から順に手前の戻って変換することで、日本語名に変換でき、
・O:酸化
・C:炭素
と命名されると覚えておきましょう。
なお、代表的な性質はこちらで詳しく解説していますので、併せて確認してみてくださいね。
CO2の構造式は?【二酸化炭素の構造式】
二酸化炭素の構造式は下記のように表されます。
炭素(C)と酸素(O)は共有結合で結合しています。

両方ともが二重結合となっていることを覚えておきましょう。
CO2の電子式は?【二酸化炭素の電子式】
さらにはCO2(二酸化炭素)の電子式についても見ていきましょう。
二酸化炭素は炭素(C)と酸素(O)が共有結合をしてできており、二酸化炭素の電子式は下記のように表されます。
二酸化炭素分子では炭素(C)及び酸素(O)がそれぞれの間で2個ずつ不対電子を出し合い、2組の共有電子対を作っています。
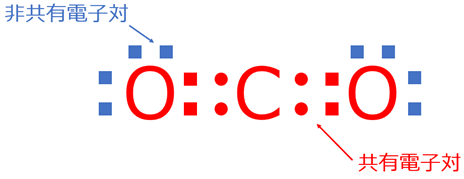
このような2組の共有電子対による共有結合のことを二重結合といいます。
この電子式を元に、構造式を覚えるとより理解が深まりますね。
CO2の分子の形は?【二酸化炭素の分子構造:立体構造】
続いてCO2(二酸化炭素)の分子の形(分子構造)も確認していきます。
二酸化炭素の分子構造(分子の形)は下記のように表されます。
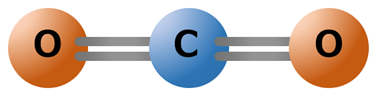
二重結合で炭素と酸素が結合された直線形状を構成しています。
こちらも上の構造式と併せて覚えておくといいです。
CO2の極性は?【二酸化炭素の極性】
さらには、CO2(二酸化炭素)の極性についてもチェックしてみましょう。
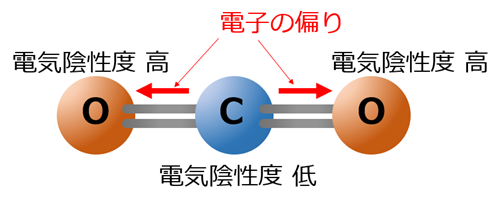
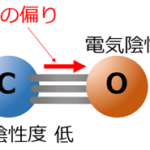
二酸化炭素を構成する炭素(C)と酸素(O)では電気陰性度に違いがあり、電気陰性度が高い酸素(O)の方に二重結合内での電子に偏りが発生します。
しかしながら、分子構造が直線形状であり、また分子構造が左右対称であるため、その電子の偏りは相互に相殺され、結果的に分子全体としては極性は発生しません。
まとめ CO2の構造式・電子式・分子の形や極性は?【二酸化炭素】
ここまで二酸化炭素の分子式、構造式、電子式、分子構造、極性について考えてきました。
内容をまとめると、
- 二酸化炭素は炭素(C)と酸素(O)が結合した化合物である。
- 結合は2組の共有電子対を形成する二重結合で結合される。
- 分子形状は直線形状である。
- 炭素(C)と酸素(O)の電気陰性度の差により電子の偏りは発生するが、分子内で相殺され、分子としては極性を持たない。
二酸化炭素という物質は地球温暖化の原因とも言われておりニュース等でもよく耳にする物質ですので、この機会に分子の構造や形状も含めて知っておくと理解が深まると思います。

コメント