科学的な解析(化学)を行う際には基本的に反応物質の電子式や構造式の理解が必要となることが多いです。
そのためさまざまな物質の電子式や構造式を理解しておくといいわけですが、なかなか覚えにくいものです。
中でもここでは、アルデヒドであるホルムアルデヒド・アセトアルデヒド・プロピオンアルデヒドの電子式と構造式をまとめていきますので、参考にしてみてください。
ホルムアルデヒドの電子式と構造式【HCHOとルイス構造式】
それでは以下で化学物質のホルムアルデヒドの電子式と構造式を確認していきます。
電子式(ルイス構造式)とは、最外殻にある電子の数を・に表すことによって分子内の各原子の種類や結合状態などを表すことができるものです。
そしてホルムアルデヒド(HCHO)の電子式は以下のように表すことができます。
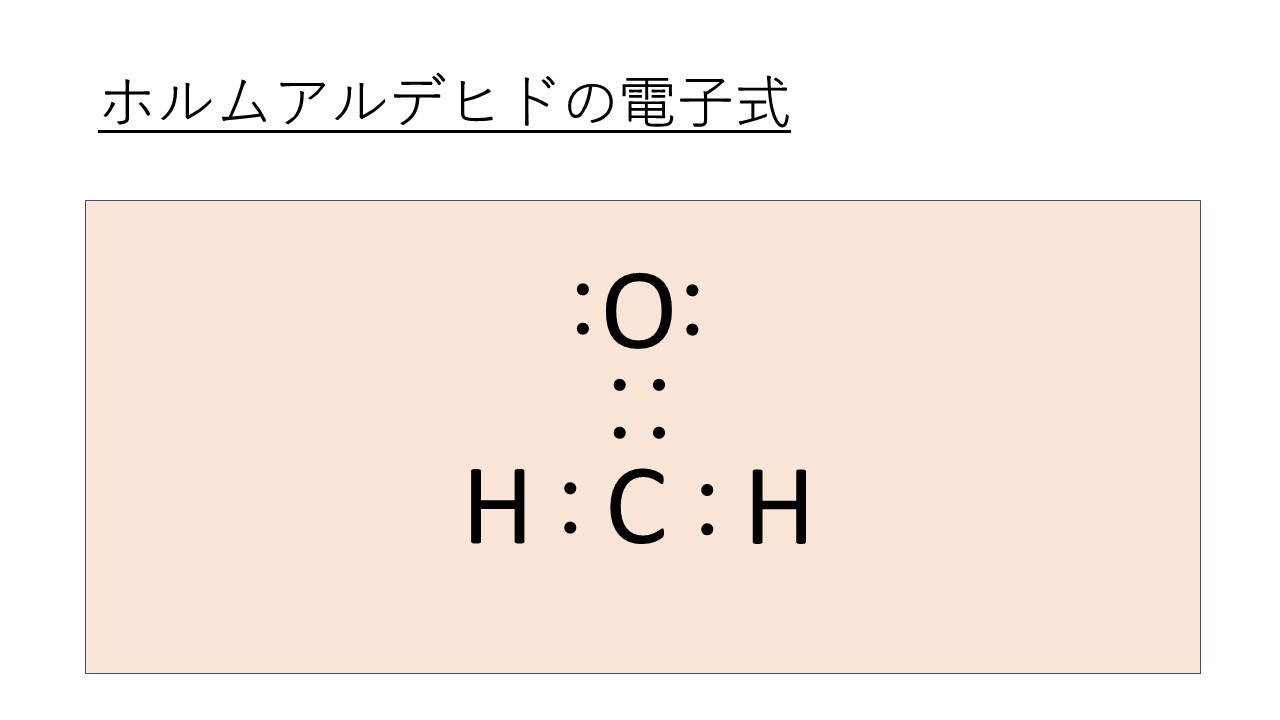
これは炭素Cの最外殻電子が4個、水素Hの最外殻電子が1個、酸素Oの最外殻電子が6個であり、アルデヒド基(CHO)を持つことからこのようになるのがわかるでしょう。
ホルムアルデヒドの構造式はこの電子式を元に考えるといいのですがホルムアルデヒドの電子式では :(共有電子対)がCO結合間で重なっていることからここが2重結合とわかります。
一方で、CH結合では:が重なっていないため、この部分では単結合となるのがわかります。
このような理由からホルムアルデヒド(HCHO)の構造式は以下のようになるのです。
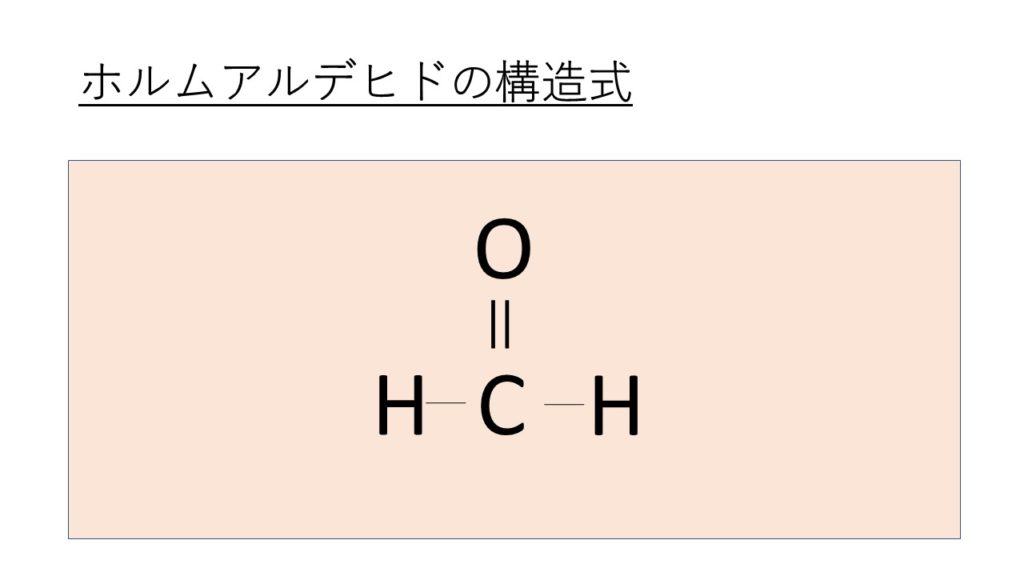
ホルムアルデヒドの電子式と構造式は有機化学を理解する上での基礎となるため理解しておきましょう。
なお、CH2O(ホルムアルデヒド)の化学式(分子式)や分子量や酸化数や示性式についてはこちらで解説していますので、併せて確認してみてください。

アセトアルデヒドの電子式と構造式【CH3CHO】
続いて炭素数がホルムアルデヒドよりも一つ多いアルデヒドの「アセトアルデヒド」の電子式と構造式を確認していきます。
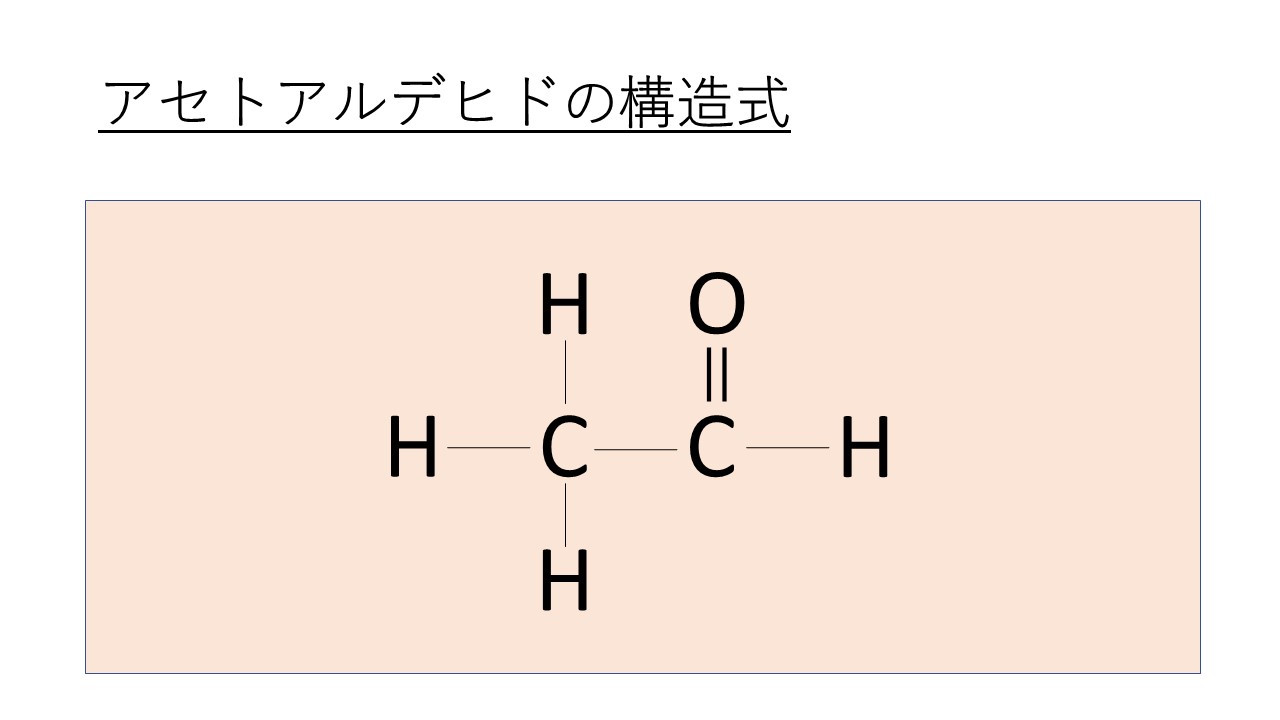
アセトアルデヒド(CH3CHO)の電子式(ルイス構造式)は以下の通りとなります。
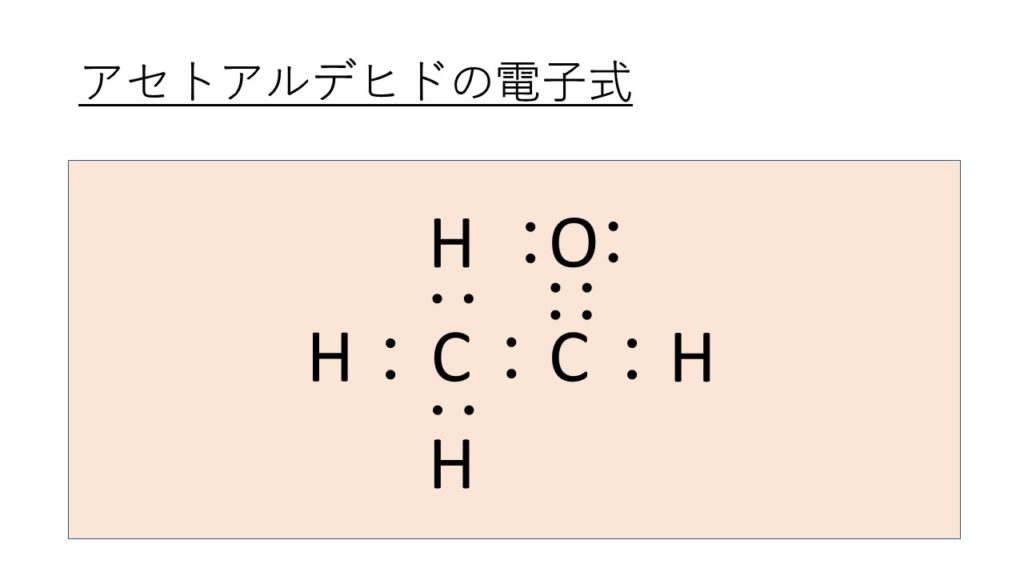
こちらも炭素Cの最外殻電子が4個、水素Hの最外殻電子が1個、酸素Oの最外殻電子が6個であり、アルデヒド基(CHO)を持つことからこのようになるのがわかります。
アセトアルデヒドの構造式はこの電子式を元に考えるとよく、 :(共有電子対)がCO結合間で重なっていること(::)からここが2重結合とわかります。
一方で、CH結合では:が重なっていないため、この部分では単結合となるのがわかります。
よってアセトアルデヒド(CH3CHO)の構造式は以下のようになるのです。
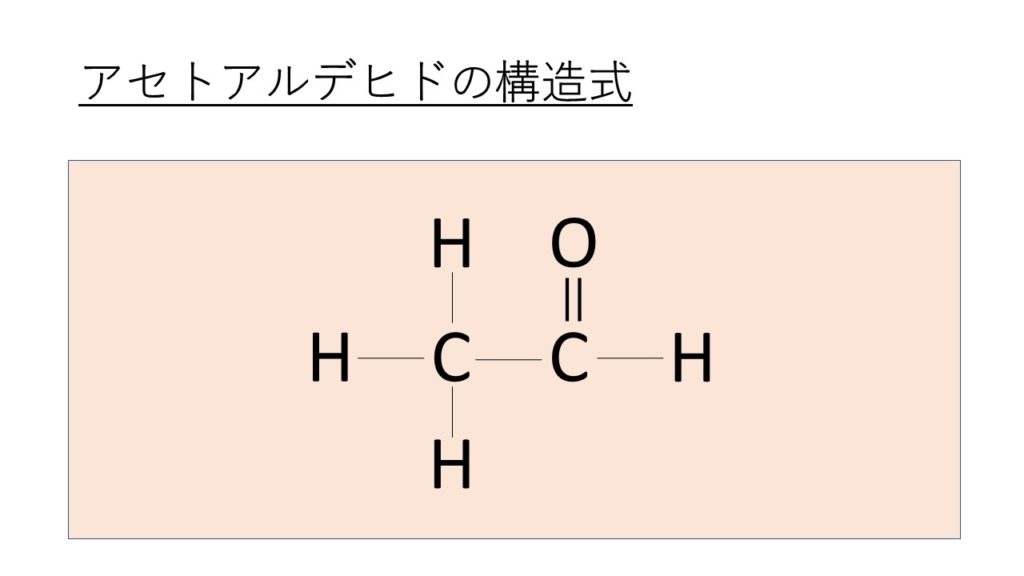
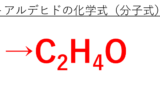
なお、C2H4O(アセトアルデヒド)の化学式(分子式)や分子量や酸化数や示性式は?酸化の化学反応式は?についてはこちらで解説していますので、併せてチェックしてみてください。
プロピオンアルデヒドの構造式【C2H5CHO】
続いて炭素数がアセトアルデヒドよりも一つ多いアルデヒドの「プロピオンアルデヒド」の電子式と構造式を確認していきます。
プロピオンアルデヒド(C2H5CHO)の構造式は炭素数が3つであること、アルデヒド基を持つことから構造式は以下のようになるのです。
※
ホルムアルデヒド、アセトアルデヒド、プロピオンアルデヒドあたりの電子式と構造式は化学を理解するベースとなるのでよく覚えておきましょう。
またそもそも上の解説のアルデヒドではアルデヒド基(CHO)を持つことと認識しておくのも今後も学習に役立ちます。
まとめ アセトアルデヒドの電子式・構造式は?プロピオンアルデヒドの構造式は?
ここではアルデヒドであるホルムアルデヒド・アセトアルデヒド・プロピオンアルデヒドの電子式と構造式について解説しました。
電子式は丸暗記するというよりも構成元素の周りの電子数を理解し、それを元に考えると効率よく覚えられます。さらに各々の構造式はこの電子式を元に描くといいです。
各種電子式や構造式を覚え、化学をもっと好きになっていきましょう。

コメント