科学的な解析(化学)を行う際には基本的に反応物質の分子量や酸化数や電離式などの理解が必要となることが多いです。
そのためさまざまな物質の分子量や酸化数や電離式を理解しておくといいわけですが、あなた覚えられていますか。
ここでは代表的な化学物質のH2O2(過酸化水素)に着目して、その分子量・酸化数・電離式や、KI(ヨウ化カリウム)との反応式などをまとめていきますので、参考にしてみてください。
H2O2の酸化数は?【過酸化水素の酸化数】
それではまずH2O2の酸化数について考えていきましょう。
H2O2の各々の酸化数はH:+1、O:-1となります。
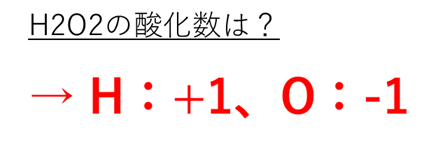
つまり(+1×2 )+(-1×2 ) = 0となり、H2O2単体での酸化数は0と収支が取れているのですね。
H2O2の際にはOの酸化数が-1となっていることに気を付けましょう。
H2O2の電離式は?【過酸化水素の電離式】
なお、H2O2の問題として「電離式」が求められるケースも多いです。
H2O2の電離式は、2H2O2 → O2 + 2H+ + 2OH-となります。
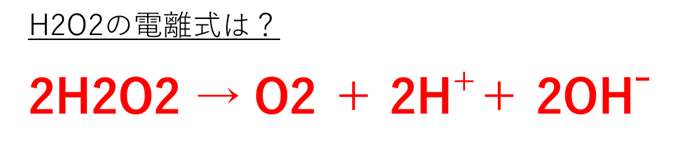
過酸化水素水は酸素と水に分離すると覚えましょう。
H2O2の分子量は?【過酸化水素の分子量】
さらには、H2O2の分子量を問われることも多いです。
結論からいいますと、H2O2の分子量は34.0です。
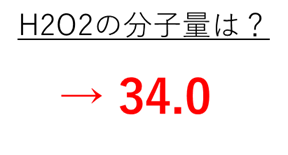
具体的には各々の値が
・H:1.0
・O:16.0
のため、(1.0×2)+ (16.0×2)=34.0と計算できるのです。
H2O2とヨウ化カリウム(KI)との化学反応式は?
さらには、H2O2(過酸化水素)とKI(ヨウ化カリウム)の化学反応式についても見ていきましょう。
ここで、硫酸を用いるのは溶液を酸性にして、水素イオンが十分に存在することで酸化反応をしやすくするためです。
まとめ H2O2の電離式や分子量、ヨウ化カリウム(KI)との化学反応式も解説!【過酸化水素】
ここでは、代表的な化学物質のH2O2(過酸化水素)に着目して、その分子量・酸化数・電離式、ヨウ化カリウムとの反応式などについて解説しました。
ややこしい化学式が多いため、この機会に覚えておくといいです。
さまざまな反応を理解し、日々の業務に役立てていきましょう。
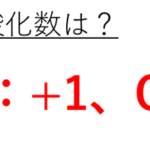
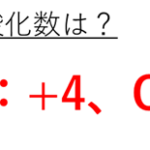
コメント