科学的な解析(化学)を行う際には基本的に反応物質の分子量や酸化数や電離式などの理解が必要となることが多いです。
そのためさまざまな物質の分子量や酸化数や電離式を理解しておくといいわけですが、あなた覚えられていますか。
ここでは代表的な化学物質のH2O(水)に着目して、その分子式、構造式、電子式、分子構造、極性などをまとめていきますので、参考にしてみてください。
H2O(水)の分子式(化学式)は?【水の分子式】
それでは以下で水の分子式(化学式)について確認していきます。
水の分子式は、水素原子(H)2つと酸素原子(O)1つが結合しH2Oと表さます。

水は分子式と組成式は同じでH2Oと表されます。
水はとても日常的な物質のため、この機会に化学式(分子式)を覚えておきましょう。
H2Oの構造式は?【水の構造式】
さらには水(H2O)の構造式も見ていきましょう。
水の構造式は下記のように表されます。

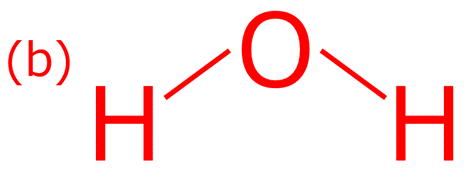
(a)のように表される場合と(b)のように表される場合があります。
どちらの表記も正しいですが、実際の分子の形状は後に解説するように(a)のように直線ではなく、(b)のように折れ曲がった形になっていることが分かっています。
ここで、水素(H)と酸素(O)は共有結合で結合していることも覚えておきましょう。
H2Oの電子式は?【水の電子式】
さらには、水(H2O)の電子式についても確認していきます。
水は水素(H)と酸素(O)が共有結合をしてできており、水の電子式は下記のように表されます。
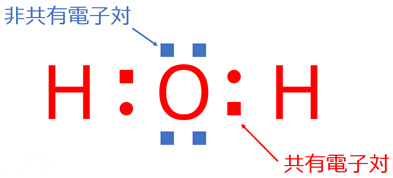
酸素(O)の持つ2つの不対電子に不対電子1つを持つ水素(H)2つが結合しています。
H2Oの分子の形は?【水の分子構造:立体構造】
さらには水の分子の形についても確認していきます。
水の分子構造は下記のように表されます。
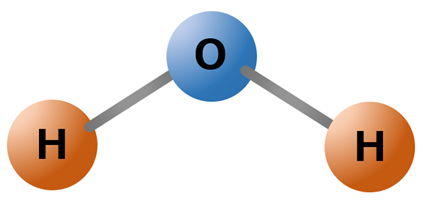
水は折れ線の分子の形になると覚えておきましょう。
H2Oの極性は?【水の極性】
さらには水(H2O)の極性も確認していきます。
結論からいいますと、水は極性があります(極性分子です)。
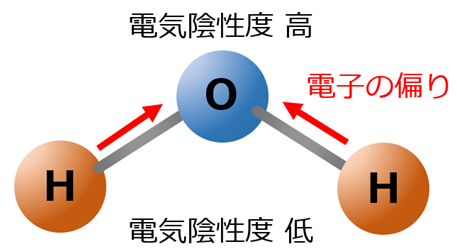
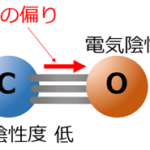
水を構成する水素(H)と酸素(O)では電気陰性度に違いがあり、電気陰性度が高い酸素(O)の方にO-H共有結合内での電子に偏りが発生し、その結果、酸素(O)側の陰性が高まり、結果的に分子全体で極性を持つことになります。
まとめ H2Oの構造式・電子式・分子の形や極性は?【水】
ここまで水の分子式、構造式、電子式、分子構造、極性について考えてきました。
内容をまとめると、
- 水は水素(H)と酸素(O)が結合した化合物である。
- 結合は共有電子対を形成する共有結合で結合され、2つの非共有電子対を持つ。
- 分子形状は直線ではない。。
- 酸素(O)と水素(H)の電気陰性度の差及び分子形状の影響で極性を持つ極性分子である。
水は生命には必ず必要な物質で、生活の中にも多く目にする機会があります。
この機会に分子の構造や形状も含めて知っておくと理解が深まると思います。
コメント